במעבדה של פרופ' ליאור גפשטיין הצליחו, לראשונה בעולם, ליצור רקמת לב פועמת מתאי גזע עובריים וגם לשלב בתוכה כלי דם. מה המרחק מכאן ועד השתלת רקמת לב מהונדסת בחולים עם אי ספיקת לב קשה? "הדרך עוד קשה וארוכה" מזהיר פרופ' גפשטיין, "אבל בינתיים, זה נראה מבטיח..."
מאת: נועם שדה עם פרופ' ליאור גפשטיין, ראש המעבדה
לחקר הלב, הפקולטה לרפואה ע"ש רפפורט, הטכניון רופא בכיר ביחידה לאלקטרו פיזיולוגיה קלינית, הקריה הרפואית רמב"ם
"רוצה לראות אותם?" שאל בסוף פרופ' גפשטיין. זו הייתה שאלה רטורית. הוא פתח את דלת האינקובאטור, בו היו מונחות צלוחיות מעבדה קטנות ועגולות, בחר אחת והניח אותה מתחת למיקרוסקופ. "הנה הם, שם במרכז.. התאים הפועמים שלנו".
מבעד לעינית המיקרוסקופ ניתן היה לראות בבירור מצבור תאים זעיר ואפרפר, שפעם בקצב אחיד, מתכווץ ונמתח, מתכווץ ונמתח, בדיוק כמו שריר לב קטנטן. גם מבלי לחשוב על הקשר המדעי הרחב - היה בזה משהו מרגש, בלתי מוסבר.
"הפועמים", הם קוראים להם במעבדה של פרופ' ליאור גפשטיין, כאילו היו אלו יצורים חיים. לפני כשש שנים (ב-2001), הם נחשפו לראשונה בפרסום מדעי, שבישר לעולם על חוקרים מהפקולטה לרפואה על שם רפפורט בטכניון, שהצליחו ליצור במעבדה רקמת לב פועמת מתאי גזע עובריים אנושיים.
"זו הייתה פריצת דרך משמעותית" אומר פרופ' גפשטיין, "עבודה ראשונה שפורסמה בעולם שבוצעה במעבדתי על ידי ד"ר יצחק קהת בשיתוף עם מעבדתו של פרופ' יוסף איצקוביץ-אלדור שהראתה שניתן ליצור במעבדה תאי לב אנושיים, שיש להם את כל התכונות של תאי שריר לב טבעיים".
תאי הלב הם התאים היחידים בגופנו הפועמים ספונטאנית בצורה מתמדת. שריר שלד לדוגמא, צריך לקבל גירוי עצבי כדי להתכווץ. אולם, יכולת השחזור של תאי הלב מאוד מוגבלת – הם לא יודעים להתחלק ולהתרבות. כך, שכל איבוד של תאי לב הוא למעשה בלתי הפיך.באירוע של אוטם שריר הלב, לדוגמא, אזור מסוים בלב לא מקבל אספקת דם כתוצאה מחסימה פתאומית של כלי דם כלילי. במקרה ואספקת הדם לרקמה לא מתחדשת תוך מספר שעות, התאים באזור הפגוע מתים והשריר הופך לרקמת צלקת שלא מתכווצת יותר. כתוצאה מכך התפקוד של הלב כמשאבה הולך ומידרדר. כאשר אובדן תאי הלב הוא משמעותי ביותר (יותר מרבע תאי שריר הלב) ותפקוד הלב מתדרדר מתחת לרמה מסוימת, מתפתחת תסמונת של 'אי ספיקת לב'. תסמונת זו אחראית ליותר אשפוזים מכל מקרי הסרטן גם יחד. למרות השיפור המשמעותי בטיפול התרופתי והלא-תרופתי בתסמונת הזו עדיין מספר החולים הסובלים ממנה ושיעורי התמותה ממשיכים לגדול. במקרים הקשים ביותר של אי ספיקת לב, הפתרון היחיד הוא השתלת לב ולאור החוסר המתמיד באיברים להשתלה, זהו פתרון מוגבל. 
פרופ' ליאור גפשטיין במעבדה לחקר הלב
תאי הלב הם התאים היחידים בגופנו הפועמים ספונטאנית בצורה מתמדת. שריר שלד לדוגמא, צריך לקבל גירוי עצבי כדי להתכווץ. אולם, יכולת השחזור של תאי הלב מאוד מוגבלת – הם לא יודעים להתחלק ולהתרבות. כך, שכל איבוד של תאי לב הוא למעשה בלתי הפיך.באירוע של אוטם שריר הלב, לדוגמא, אזור מסוים בלב לא מקבל אספקת דם כתוצאה מחסימה פתאומית של כלי דם כלילי. במקרה ואספקת הדם לרקמה לא מתחדשת תוך מספר שעות, התאים באזור הפגוע מתים והשריר הופך לרקמת צלקת שלא מתכווצת יותר. כתוצאה מכך התפקוד של הלב כמשאבה הולך ומידרדר. כאשר אובדן תאי הלב הוא משמעותי ביותר (יותר מרבע תאי שריר הלב) ותפקוד הלב מתדרדר מתחת לרמה מסוימת, מתפתחת תסמונת של 'אי ספיקת לב'. תסמונת זו אחראית ליותר אשפוזים מכל מקרי הסרטן גם יחד. למרות השיפור המשמעותי בטיפול התרופתי והלא-תרופתי בתסמונת הזו עדיין מספר החולים הסובלים ממנה ושיעורי התמותה ממשיכים לגדול. במקרים הקשים ביותר של אי ספיקת לב, הפתרון היחיד הוא השתלת לב ולאור החוסר המתמיד באיברים להשתלה, זהו פתרון מוגבל.
פרופ' גפשטיין מכיר את הבעיה ממקור ראשון. הוא רופא קרדיולוג במקצועו, המתמחה בתחום החשמלי של הלב. "זה הייחוד של רופא חוקר", מסביר גפשטיין, "שהוא נתקל בבעיות קליניות ומנסה למצוא להן פתרונות ברמה המחקרית, בניגוד לחוקר שהוא רק חוקר או רופא שהוא רק רופא. כך עלה הרעיון לנסות לגדל תאי לב במעבדה - במקום להשתיל לב שלם, למה לא להחליף רק את רקמת הצלקת הפגועה ברקמת לב חדשה?".
הבחירה בתאי גזע עוברים הייתה די ברורה: בניגוד לתאי גזע בוגרים, את תאי הגזע העובריים קל לגדל במעבדה. הם יכולים להתחלק וליצור כמויות אדירות של תאים ויש להם גם יכולת להתמיין ולהפוך לכל רקמה בגוף. בשלב ראשון תאי הגזע העובריים מגודלים בצורה הלא ממוינת, בהמשך מעבירים אותם לתמיסה, שבתוכה מתחילה התמיינות למגוון רקמות. בשלב זה מוסיפים פקטורים מסוימים מתוך מטרה לדחוף אותם לכיוון התמיינות מסוים, כך שחלק מהתאים שיתקבלו יהיו תאי לב.
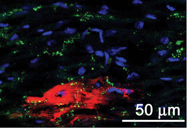
תאי הלב המושתלים המשמשים כקוצב ביולוגי
אולם, העובדה שהתקבלו תאים פועמים עדיין לא הספיקה כדי לקבוע בוודאות שאכן מדובר בתאי לב. "הרצנו אותם תחת מגוון בדיקות" משחזר פרופ' גפשטיין, "ראינו שהם מבטאים גנים וחלבונים ייחודיים של תאי לב והם בעלי מבנה ייחודי של תאי לב. בנוסף נמצא שלתאים תכונות פונקציונאליות של תאי לב אנושיים. ניתן היה לרשום מהם פעילות חשמלית בדומה לא.ק.ג. והם גם הגיבו להורמונים שונים, כך שאם נותנים להם אדרנלין, לדוגמא, הם מתחילים לפעום מהר יותר".
"השאלה הבאה ששאלנו את עצמנו הייתה: האם התאים הללו קשורים יחד ופועלים בסנכרון כרקמה פונקציונאלית אחת? לשם כך השתמשנו במערך אלקטרודות שרשמו פעילות חשמלית מהתאים הפועמים וראינו שאכן לא מדובר רק בתאי לב בודדים, אלא נוצרת רקמה של תאי לב הפועמת בסנכרון".
מעבדת תאי הגזע של פרופ' גפשטיין, הנמצאת בקומה ה-10 של בניין רפפורט שליד רמב"ם, מטעה קצת במבט ראשון. חדר אחד לא גדול במיוחד, שבו כמה מדפים עמוסי מבחנות וצנצנות, ואליו צמודים עוד שלושה חדרים קטנים. משום מה, לא כך מצטייר בדמיון אחד המרכזים המובילים בעולם בתחום הנדסת הרקמות, בו הופכים מדע בדיוני למציאות. אבל בדיוק כאן, עשו המדענים הישראלים את מה שכל כך הרבה מדענים אחרים בעולם ניסו ולא הצליחו.
רקמת התאים הפועמים היוותה קפיצת מדרגה בפיתוח. היא אפשרה לחוקרים להתחיל ולערוך ניסויים על רקמה שלמה של תאי לב, מה שעד כה היה בגדר חלום בלבד. כעת, ניתן היה להשתמש בתגלית כדי לבדוק למשל, איך משפיעות תרופות חדשות על רקמת לב. מדובר ביישום שעשוי לחסוך מיליוני דולרים לחברות המפתחות תרופות רק על רקמת לב אנושית. אולם, הדרך למטרה הראשונית של הפיתוח – השתלת 'הפועמים' ברקמת צלקת של לב אנושי לטיפול באי ספיקת לב - עוד ארוכה.
פרופ' גפשטיין: "קיימות עוד הרבה בעיות שיש לפתור: במהלך ההתמיינות נוצרים מספר סוגים של תאים ורק מיעוט מתאי הגזע הופכים להיות תאי לב. אנחנו מנסים לפתח מערכות שיגבירו את ההתמיינות הלבבית. בהמשך, צריך יהיה לפתח שיטות שיעזרו לברור החוצה רק את תאי הלב. בעיה משמעותית נוספת היא כמותית, צריך יהיה בעתיד לפתח שיטות תעשייתיות על מנת לייצר מיליארדי תאים שכאלה, כי היום במעבדה אנו מסוגלים לייצר סדר גודל של מיליוני תאי לב בלבד. ועוד לא דיברנו על הבעיה של דחייה חיסונית של התאים והאם התאים המושתלים ישרדו בסביבה העוינת בתוך צלקת...? מדובר בעוד הרבה עבודה קשה והרבה דם, יזע ודמעות.
"עכשיו, אנו מתמודדים עם השאלה כיצד נשתיל את התאים בלב של החולים? קיימות שלוש אפשרויות ואנחנו עובדים בכל הכיוונים: הראשונה, במהלך ניתוח, להשתיל את התאים ישירות לרקמת הצלקת בלב. האפשרות השנייה היא להזריק את התאים לרקמת הצלקת בתהליך של צנתור. האפשרות השלישית היא דרך טכנולוגיה של הנדסת רקמות. בכיוון הזה אנחנו עובדים בשיתוף פעולה עם מספר קבוצות בטכניון ובעולם. כך לדוגמא, יש לנו פרויקט משותף עם ד"ר שולמית לבנברג מהטכניון, שהצליחה לגרום להתמיינות תאי אנדותל (התאים המצפים את חלל כלי הדם) מתאי גזע עובריים. רק בתחילת השנה הנוכחית פורסמה עבודה של ד"ר אורן כספי ממעבדתי והמאסטרנטית איילת לסמן ממעבדתה של ד"ר לבנברג, שהצליחו לשלב את תאי הלב האנושיים המתקבלים עם תאי האנדותל וליצור רקמת לב מהונדסת אנושית, המכילה תאי לב עם כלי דם ופועמת כיחידה אחת..הרקמה שהתקבלה בשיטות של הנדסת רקמות כבר מתחילה להזכיר קצת מבנה יותר מסובך של איבר".
עד כמה אתם רחוקים מיצירת איבר, לב שלם ופועם?
פרופ' גפשטיין: "אנחנו מנסים לחקות בצורה פשטנית את מה שקורה באופן טבעי ומדהים בכל עובר ותינוק שנולד. מאוד קשה לעשות זאת. אמנם הצלחנו ליצור רקמת לב פועמת, אבל איבר שלם הוא מבנה מורכב המכיל מגוון של רקמות מסוגים שונים, המשולבים יחד בצורה שעדיין אי אפשר לחקות אותה במעבדה. התהליך הזה מלמד אותך להיות מאוד, מאוד צנוע במה שהאדם יכול לעשות".
ומה לגבי העתיד?
פרופ' גפשטיין: "יכול להיות שבעוד עשר שנים תבוא לראיין אותי שוב ואף אחד מהרעיונות שהזכרנו בראיון לא יגיע לכדי מימוש קליני . אבל כך מתחילים תהליכים מחקריים ובינתיים, זה נראה מבטיח. רק העתיד יגיד לאן זה יוביל".

