אולטרסאונד ממוקד (FUS ) הוא טיפול חדשני ולא פולשני לסובלים מרעד ראשוני או רעד בשל מחלת פרקינסון.
הטיפול ברעד ראשוני בעזרת אולטרסאונד פותח ברמב"ם לפני מספר שנים, והוכנס לשימוש בארץ דרך סל התרופות בשנת 2013. עבור חולים עם רעד ראשוני הטיפול הינו בסל התרופות.
המכון להפרעות תנועה ברמב"ם נחשב למרכז מוביל בטיפול בפרקינסון ומטופלים רבים מישראל ומכל העולם פונים לקבל את הטיפול במכון, כולל מטופלים מארה"ב, קנדה, אוסטרליה, רוסיה, הולנד, ברזיל ועוד.
השיפור ברעד ובדרך כלל אף העלמות מיידית של הרעד בעקבות טיפול באולטרסאונד ממוקד דווח במאות מאמרים בכתבי עת הרפואיים המובילים בעולם.
צפו בד"ר אילנה שלזינגר מרמב"ם מסבירה בתכנית "סטטוסקופ" של רשת 13 על רעד ראשוני וטיפול ה- FUS:
למה לבצע את הטיפול ברמב"ם?
רמב"ם נחשב כיום למרכז עם התוצאות הטובות ביותר בעולם בטיפול זה. הוא נחשב למרכז בו מתבצע הטיפול ביעילות הגבוהה ביותר עם תופעות הלוואי הפחותות ביותר. בשל נתונים אלה פונים לרמב"ם חולים מכל רחבי הארץ והעולם, כדי לקבל את הטיפול מהצוות המקצועי במכון להפרעות תנועה.
מהו רעד?
רעד הוא בעיה נוירולוגית. כאשר הרעד הוא בדרגת חומרה בינונית עד קשה הוא פוגע באיכות החיים. לעתים קרובות הרעד אינו סימטרי וחמור יותר בצד אחד של הגוף. רעד בינוני-קשה מפריע לביצוע פעולות יומיומיות כגון אכילה, שתייה, כתיבה ופעולות רבות נוספות המחייבות טיפול. עם השנים עלול הרעד להחמיר ולגרום לנכות. מטופלים רבים, עם רעד משמעותי, אינם מגיבים לתרופות ועשויים לשקול הליך ניתוחי, לרבות השתלת אלקטרודות לגירוי מוחי.
המכון להפרעות תנועה ופרקינסון ברמב"ם מציע טיפול ייחודי המבוצע על ידי מערכת אולטרסאונד במכון ה- MRI ללא צורך בניתוח, ללא חתכים וללא השתלות. הטיפול בפרקינסון מביא בדרך-כלל להקלה משמעותית ומידית ברעד.
מהו אולטרסאונד ממוקד לטיפול ברעד ראשוני?
הטיפול באולטרסאונד ממוקד הוא טיפול זעיר פולשני העושה שימוש בגלי אולטרסאונד באנרגיה גבוהה, לצריבה של חלק זעיר במוח, המשמש כתחנת ממסר להעברת אותות חשמליים. קרני האולטרסאונד ממוקדות לאזור מסוים במרכז המוח (התלמוס). הקרניים מחממות את האזור עד לצריבה נקודתית מבלי להשפיע על שאר רקמת המוח. כך מופסקת ההעברה הבלתי תקינה של האותות החשמליים במוח והרעד נרגע.
הטיפול משלב שימוש בגלי אולטרסאונד עם הדמיית תהודה מגנטי ת-MRI. שילוב זה מאפשר לרופאים לכוון את הגלים למטרה בצורה מדויקת מאוד ולנטר את השפעתם על החולה בזמן אמת. כך מותאם הטיפול אישית לכל חולה וחולה.
מה קורה במהלך הטיפול ברעד ראשוני?
בזמן הפעולה המטופל שוכב בתוך מכשיר ה- MRI. בכדי להבטיח שהראש לא יזוז במשך הטיפול, מורכבת על ראש המטופל מסגרת מיוחדת לקיבועו. הרופא בוחן את מבנה המוח ומגדיר את מוקד הטיפול. גלי האולטראסאונד מכוונים אל מוקד זה בטמפרטורות הולכות ועולות תוך ניטור קפדני של החולה בכדי לוודא הקלה ואף העלמות של הרעד. תוך כדי הטיפול החולה נבדק פעמים חוזרות בכדי למנוע תופעות לוואי. הטיפול נמשך כ 2-3 שעות, ללא הרדמה והפסקת הרעד או השיפור המשמעותי מורגש מיד בסיומו.
מה קורה לאחר הטיפול?
לאחר הטיפול נשאר המטופל להשגחה של 24 שעות בכדי לוודא שאין תופעות לוואי. למחרת, מבוצעת בדיקתMRI נוספת. ברוב המטופלים, לאורך חודשים ואף שנים, הרעד לא חזר. מטופלים שחוו חזרה של הרעד, הרי שהרעד היה כמעט תמיד פחות חמור מאשר לפני הטיפול. ישנם מספר מטופלים בהם חזר הרעד לקדמותו.
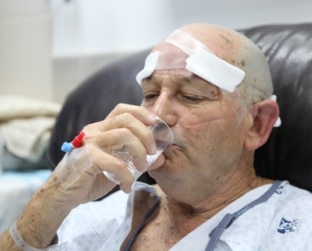
המטופל שותה כוס מים בעצמו מייד לאחר הטיפול.

בתמונה: קווים שצוירו בתוך ספירלה על ידי מטופל - לפני הטיפול (מימין), מיד לאחר הטיפול (באמצע) ושנה לאחר הטיפול (משמאל).
מהם הסיכונים?
מהלך הטיפול קיימת אפשרות לנזק לרקמות בסמוך לאזור הטיפול. נזק אפשרי זה מופחת באמצעות בקרה קפדנית במשך הטיפול. תופעות הלוואי המופיעות בזמן הטיפול כוללות בעיקר כאב ראש והרגשת סחרחורת שבדרך כלל חולפות בתום הטיפול. לאחר הטיפול יתכנו בחלק מהמטופלים תופעות לוואי הכוללות בין השאר תחושה של אי יציבות בהליכה, חוסר שווי משקל בהליכה, הפרעה בקואורדינציה ביד והפרעה בחוש הטעם. ברוב החולים, תופעות אלה חולפות לאחר חודש אך במקרים בודדים הם נותרו.
מהם יתרונות הטיפול באולטרסאונד ממוקד לטיפול ברעד ראשוני ?
- הטיפול מביא להקלה מידית ומתמשכת ברעד אצל רוב המטופלים
- שיפור מיידי באיכות החיים אצל רוב המטופלים
- אין צורך בחתכים בגולגולת
- אין צורך בהשתלת גוף זר
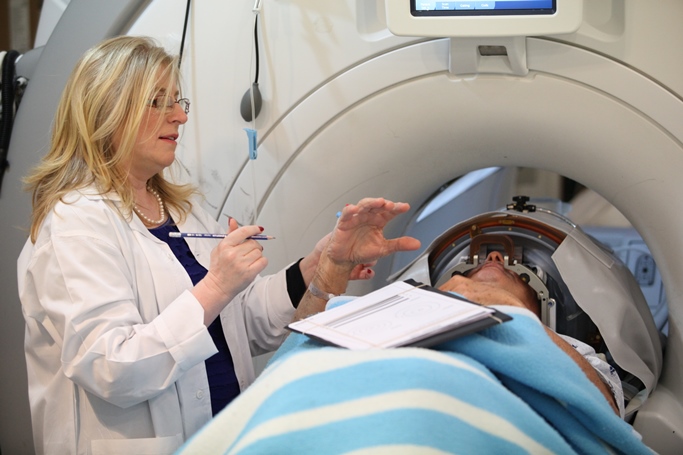
ד"ר שלזינגר בודקת את הפציינט מספר פעמים במהלך הטיפול לצורך ניטור ההליך הרפואי
מהם הסיכונים?
במהלך הטיפול קיימת אפשרות לנזק לרקמות בסמוך לאזור הטיפול. נזק אפשרי זה מופחת באמצעות בקרה קפדנית במשך הטיפול. תופעות הלוואי המופיעות בזמן הטיפול כוללות בעיקר כאב ראש והרגשת סחרחורת שבדרך כלל חולפות בתום הטיפול. לאחר הטיפול יתכנו בחלק מהמטופלים תופעות לוואי הכוללות בין השאר תחושה של אי יציבות בהליכה, חוסר שווי משקל בהליכה, הפרעה בקואורדינציה ביד והפרעה בחוש הטעם. ברוב החולים, תופעות הלוואי האלה חולפות לאחר חודש אך במקרים בודדים הם נותרו.
סיפורו של מטופל ה- FUS הראשון בישראל
בסרטון: סיפורו של סמי זנגי, הראשון במדינת בישראל שעבר טיפול ברעד באמצעות אולטרסאונד ממוקד, בשנת 2013.
לפרטים נוספים ולקביעת תור – צרו קשר בתחתית העמוד עם המכון להפרעות תנועה ברמב"ם.
לקריאת כתבה במגזין "אדם" של הקריה הרפואית רמב"ם: "לעומק המוח" >
הרעידות הפסיקו אחרי 15 שנה: סיפורה של הספרית שיכולה שוב לאחוז במספריים>
مقابلة تلفزيونية مع الدكتور رافي حداد من موسى بن ميمون حول العلاج بالموجات فوق الصوتية المركزة (FUS)>
שאלון התאמה לטיפול
מטופלים המעוניינים לבחון התאמתם לטיפול אולטרסאונד ממוקד- FUS מתבקשים למלא שאלון זה ולהחזירו על פי הפרטים בטופס.
להורדת שאלון התאמה לטיפול FUS >

